科学探秘:细胞核起源之谜
- 财经
- 6天前
- 120
人生小哲理干细胞者说
物品和文化
我们生活在一个物品来不及
形成文化就被淘汰的时代
正文
一个神奇的数值揭开一个世纪之谜,且不是天方夜谭?……从原核生物到真核生物,基因组的DNA总量大约增加了3.5个数量级。因此,仅仅用偶然的吞噬、共生或寄生来解释真核生物的起源无论如何是难以让人信服的!其实,正是内共生理论将人们推入了歧途,因为这绝对无法解释在原核与真核之间为何呈现出如此巨大的基因组差异……
1. 真核——真的是靠吞噬起源的吗?
目前提出的关于真核生物起源的最流行的理论就是所谓的内共生学说。在生物界,吞噬导致共生的现象可能客观存在,有些共生可能较为松散(一眼就能看出两者的区别,如图1),有些共生甚至连痕迹都难以觉察到,如真核细胞的叶绿体和线粒体。
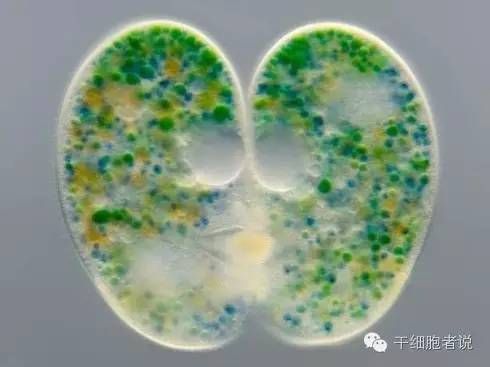
图1纤毛虫( )与藻类的共生现象(x 160倍)(来源:维姆-范-伊格蒙德)
但是,按照一般的想象,靠吞噬作用获得DNA似乎是困难的,因为如果能消化细胞壁,那里面的DNA也可能早就被破坏了。如果是这样的话,那即便是吞噬,DNA也应该是吞噬者的,但问题就来了,吞噬者的核从何而来呢?当然,如果被吞噬者幸运地存活下来了,情况可能就不一样了,即一旦它们与吞噬者形成了共生关系,两者之间的基因交流或整合就有可能了。当然,当两个不同物种形成寄生关系时,亦可能发生类似的基因交流与整合。
此外,像绿藻这样的真核藻类是如何形成的呢?即便假设吞噬者是真核的,由于吞噬者应该是动物性的,那吞噬者的细胞壁是如何转化成绿藻这样的植物性细胞壁的呢?而植物和动物的细胞壁是绝然不同的。再退一步,即便承认真核生物是一种由吞噬、共生或寄生形成的不同物种的嵌合体,但这也并未解决核的形成机制。迄今为止,几乎所有的假说都停留于推测真核起源的可能途径,而对演化的动因则鲜有涉及。
2. 生命演化的趋势——DNA链不断延伸
生命的演化伴随着基因组的扩增(复杂化)是不争的事实,特别是从原核演化到真核。这如何才能实现呢?多倍化以及细胞之间遗传物质的交流或重组可能是重要途径。譬如,细胞分裂时,如果染色体复制了但细胞未能分开,就可能出现多倍化(这样的过程依然还在自然发生,且在人的诱导下快速地发生),这也称之为同源多倍体(),而由不同物种杂交能产生异源多倍体()。在同一个细胞中,不同DNA链也可能会自动连接起来。
真核应该是基因组大型化的必然产物。如果细胞将绝大部分DNA集中在被核膜包裹的区域就形成“核”,它在细胞有丝分裂时期呈现独特的“染色体”现象——此时DNA高度聚集,容易被碱性染料(如龙胆紫和醋酸洋红)着色。而在分裂间期时,DNA分散成细丝状,称之为染色质。
这样,所谓真核,就是细胞的绝大多数DNA集中分布在了这样一个区域,且十分致密,但它也依然是一样性质的DNA。为什么真核要在核膜中?也许是一种秩序化管理的需要吧,在这里,是速度和秩序孰重孰轻的问题:在简单的细菌那里,速度优先,而在复杂的真核生物那里,秩序优先。细菌细胞由于没有核膜,DNA的复制、RNA的转录与蛋白质的合成可同时进行,而真核细胞的这些生化反应在时空上被分隔开来,但便于有序管控。但是,过分强调核膜对真核生物演化的重要性就会迷失。此外,细菌的DNA没有内含子,满足了快速复制的需求。原核细胞演化出内膜系统,不需要太大的奥妙,因为,生命最不缺少的就是膜,生命的诞生之旅亦是从膜开始的。
3. DNA链不断延伸的必然结果——压缩
无论细胞分裂看起来多么复杂而神奇,但本质就是如何将承载遗传信息的DNA准确地分配到子代细胞中去。随着生命从简单到复杂的演化,基因组的大型化在所难免,其结果就是DNA链不断延伸,这迫使DNA进行立体结构上的调整——①将DNA集中在一定的区域并用膜隔离开来,②将长长的DNA拆成若干段,即若干染色体;③对链状DNA进行压缩,通过与组蛋白的合作,成功压缩了很多倍,看上去非常的致密。
极端地说,真核的形成过程就是一种DNA的压缩过程!这是如何进行的呢?染色体结合有两种蛋白质:组蛋白(一种低分子量的碱性蛋白质)和酸性蛋白质。在真核细胞的有丝分裂过程中,与组蛋白耦联的DNA分子的压缩能力是十分惊人的(图2)。DNA双螺旋在每个组蛋白8聚体表面盘绕约1.75圈(长约140个碱基对)构成核小体。相邻核小体之间有长约50~60个碱基对的DNA连接线,在相邻的连接线之间结合了一个H1组蛋白分子。DNA似绳,组蛋白似珠,就像成串的珠子一样,这就是染色体的一级结构,在这里,DNA分子大约被压缩了7倍。螺旋体是染色体的二级结构,每一周螺旋包括6个核小体,这里的DNA被压缩了6倍。螺旋体进一步螺旋化,形成超螺旋管,即染色体的三级结构,这里的DNA被压缩了40倍。超螺旋体再折叠盘绕形成染色单体(四级结构),两条染色单体组成一条染色体,这里的DNA再被压缩了5倍。这样,DNA分子一共被压缩了7×6×40×5=8400倍!
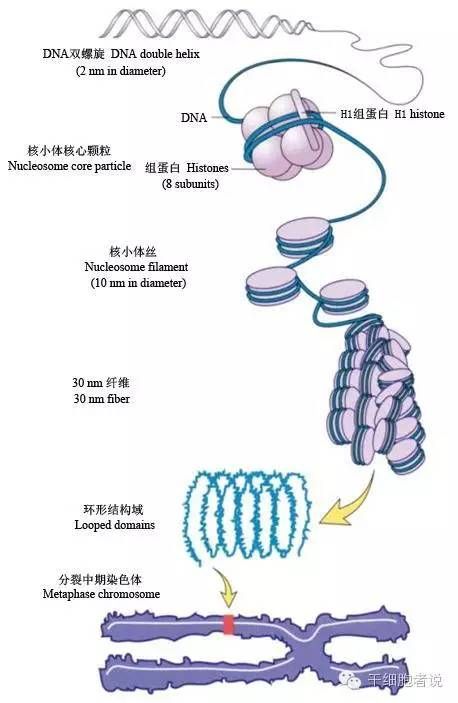
图2 DNA压缩成染色体的过程
4.真核生物DNA的压缩原理
再来看看这种DNA的压缩与基因组演化之间的关系。一般可用C值(C Value)来度量一种生物的基因组的大小,它指一种生物的单倍体基因组的DNA总量。细菌和古菌的C值(单位pg)的中位值约在10-3–10-2之间,而真核生物约在1-10之间,高约3个数量级。绝大多数C值落于中位数±1.5个数量级之间。此外,真核细胞略为原核细胞直径的10倍。若考虑中位数及其上限偏移,以及细胞直径一个数量级的差异,真核生物DNA的压缩倍数大约应该是3.5个数量级(图3),谢平(2016)将此称之为真核生物DNA的压缩原理( )。这与现代真核生物的DNA压缩比( ratio)惊人地一致!譬如,人的染色体中DNA分子伸展开来的长度平均约为几个厘米,而染色体被压缩到只有几纳米长(1 cm = 107nm)。原核生物的C值与真核生物中的原生动物和真菌亦有交集,特别是与原生动物的交集更深,这难道意味着它们可能就是真核生物的祖先吗?
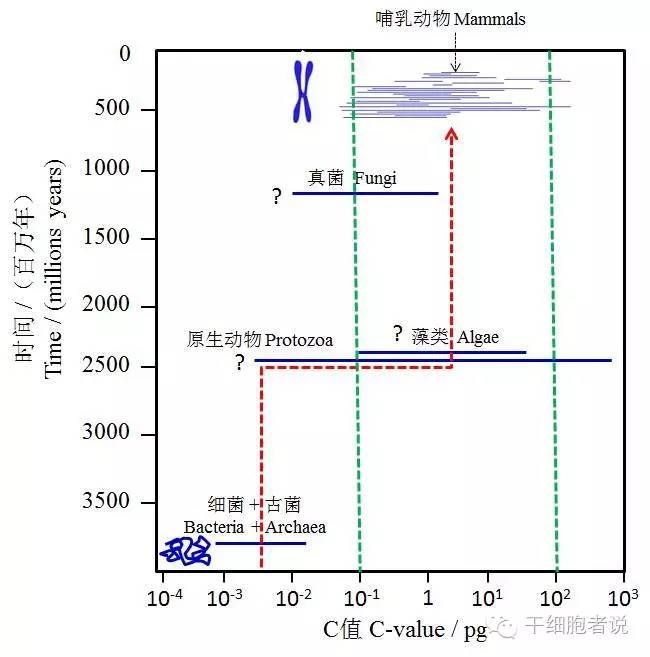
图3根据各类生物的C值推测真核生物DNA的压缩原理,带箭头的红色虚线表示C值中位数的演化轨迹,绿色虚线表示大多数真核生物C值的主要分布区间,问号表示该类生物起源的年代仍然存在争议,C值来源于(引自:谢平2016)
值得注意的是,从C值的中位数来看,原核生物与真核生物之间相差多达3个数量级,因此,仅仅用一次偶然的吞噬、共生或寄生来解释真核生物的起源无论如何是难以让人信服的,而更关键的问题是我们还需要解释真核生物的基因组为何急剧增大了。这可能与我们熟知的DNA的复制错误或多倍化现象不无关系,当然并非完全排除不同种类个体之间的侧向的基因流动或整合的可能贡献。不难理解,DNA压缩机制的成型应该就是迈向真核生物的关键一步,这自然还伴随了细胞内部的结构分化、更为精巧而复杂的细胞分裂机制的发展,等等。为了支撑大型真核细胞,必须进行大量的革新,这被大量新基因的涌现所佐证。
从生态上来说,蓝细菌光合放氧推进的大气氧浓度的上升可能是复杂而耗能的真核生物出现的重要前提,因为与厌氧代谢相比,有氧代谢的效率大大提升,而生命的复杂化需要这样的能量支撑。因此,吞噬、共生或寄生带来的生命复杂化可能仅仅是一个小小的插曲,它们虽然是真实的,且不同物种的DNA亦可能出现一定的整合,但这依然难以解释大小相差数个数量级的核的起源问题。
5. 真核生物的祖先之争
真核生物不会从天而降,它从更原始的原核生物演化而来亦是不争的事实。而分子进化生物学家长期纠结于真核生物到底源自真细菌还是古菌这样的问题。他们通过基因组序列的比对发现,真核生物的一部分基因(如信息相关基因)与古菌相似,而另一部分基因(如胞质功能基因)与真细菌相似,因此认为真核生物源自真细菌和古菌的融合()或内共生。但事实上,所有的生物都具有一个共同的祖先,因此,某一个后生物种均或多或少携带有若干祖先物种的基因,而这并不能意味它就是由这些祖先物种融合而来的。况且,不同微生物之间的横向基因流动( )手段众多且十分频繁,如果以地质年代而计,这样的变异速率是十分惊人的。
微生物其实就是一些临时拼凑的物种,虽然这类研究并非毫无意义,但至少对解释核的起源难以派上用场。试问,对那些被转来转去的基因,我们如何知道谁才是它的原创之主呢?恕我直言,试图用基因序列来确定所谓原核生物的亲缘关系以及为此精心编造的算法或故事或许只会是一种徒劳!
除了极少数的过渡类型外,细菌没有核膜,染色体DNA一般为单环的不规则体,也称之为拟核()。细菌的染色体DNA偶尔也有呈单线性的(如博氏疏螺旋体 )。拟核主要由DNA组成,亦含有少量的RNA和蛋白质(它们好像主要是mRNA和转录因子蛋白)。驱动核酸时空组织的拟核相关蛋白(- ,NAPs)与真核的组蛋白完全不同,拟核的DNA结合蛋白不形成核小体()。
6. 如何将DNA分配到子细胞中去?
细菌在二分裂期间,复制完的子染色体分别移动到细胞的相反的末端,其机制还不甚清楚,但蛋白质可能将子染色体牵引到了细胞质膜的特定位置(图4上)。在大部分真核生物中,在核外形成纺锤体(),在有丝分裂期间,核膜溶解,微管将染色体分离(图4下),之后核膜重新形成。
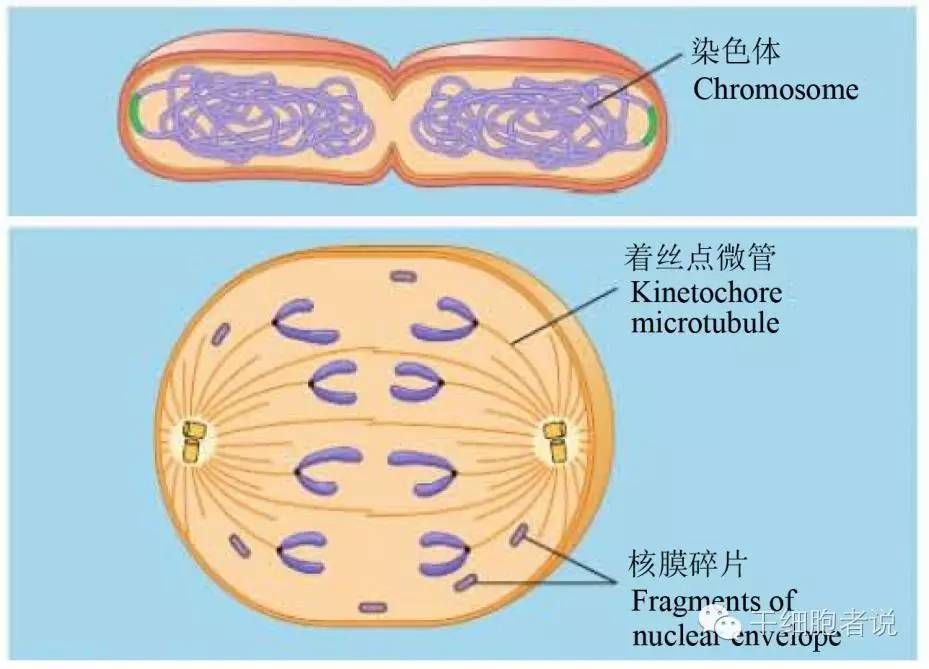
图4原核(上图,大肠杆菌 coli)和真核(下图)细胞的分裂比较(引自 and Reece 2008)
需要指出的时,无论是原核还是真核细胞,子染色体都必须要借助特定的蛋白质锚定到细胞质膜上,这样才能将DNA正确地分配到两个子细胞中去。只是在原核细胞中,这种机制较为简单,而在真核细胞中,由于要将众多的染色体同时分开,因此演化出了复杂的纺锤体结构,但也是要连接到质膜上。或者说,在原核细胞中,不需要那么复杂即可。
在现存的生物中,能找到原核和真核之间的过渡类型,可将它们视为细胞结构化过程的中间产物。譬如,浮霉菌门()和海绵杆菌门()的拟核被双层膜所包裹(类似于真核),且具有胞内膜结构(e- )。
7. 细胞核起源的压缩与结构化假说( and )
谢平提出了一个关于细胞核起源的新学说——压缩与结构化假说,认为细胞核起源自基因组复杂化的诱导,即在大气逐渐氧化的背景下,地球上的生命(无论是形态结构,还是遗传信息)加速了从简单到复杂的演化历程,可能主要由于DNA的复制错误或多倍化并在一定程度上叠加了不同种类之间的各种侧向基因转移方式以及内共生融合()等导致了一些原核细胞基因组的大型化。这一方面需要骨架蛋白的强化来支撑更大的细胞体积,同时通过个体生存的随机性筛选,细胞内部逐渐结构化,从而形成了复杂的内膜系统——细胞器,被膜包裹的核及其在细胞分裂中的分离方式亦是这种结构化的产物。核的成型及有丝分裂的出现主要是为了满足将巨大的DNA分子准确地分配到子代中去的需求,这里,如何将长链DNA有效地压缩(借助组蛋白)成若干染色体以及如何将多个染色体同时分离(借助纺锤体)是核演化的关键。核膜的形成虽然并非轻而易举,但亦不会困难无比,膜有多种可能的来源,譬如,原核细胞分裂时DNA就得锚定在细胞膜上。其实,生命就起源自膜耦联的光化学过程,细胞亦能产生各种各样的膜。从本质上来看,包括核膜在内的细胞内膜系统就是为了实现对复杂生化系统进行秩序化管控,或者说,秩序化是通过细胞内部的模块化得以实现的。这虽然可视之为一种自演化模型,但在压缩原理和结构化等的基础上,诠释了核演化的动因与本质(谢平2016)。
结语:
DNA压缩机制的成型应该就是迈向真核生物的关键一步,这当然还需要细胞内部的结构分化、精巧而复杂的细胞分裂机制等的发展。一个神奇的数值——3.5个数量级既是真核生物与原核生物C值的差异,亦是现代真核生物的DNA压缩比( ratio)。这绝不是偶然而无关的巧合!它是细胞核起源的数字机密,是被纷繁杂沓与变幻莫测的表象所掩盖的演化真谛!
参考文献
Cell:DNA复制的起源
对于DNA复制来说,其基本单元复制子受到顺式作用元件和反式激活因子的调控,尽管真核生物基因组的体积和复杂性不断提高,但是真核DNA复制依然遵循着复制子模型中的最基本规律和原则。近期Cell杂志以“ of DNA ”为题,追溯了DNA复制的起源。
DNA复制意义重大,这一途径是细胞分裂前的必要步骤,而且也是绝大多数化疗药物的作用靶标,这些药物通过破坏DNA复制来杀死肿瘤细胞。因此解析DNA复制机制对于基础研究和临床研究来说都科学家们的焦点。
DNA复制的界线
真核生物的染色体复制是有时间顺序的,人们将其称为复制时间程序(- )。在哺乳动物中,复制时间存在着细胞类型特异性。而且在发育过程中,至少有半数基因组会发生复制时间的改变。这种改变主要是基于400–800kb的单元,即复制结构域( )。
来自佛罗里达州立大学的一项新研究首次确定了这些单元的边界,这一成果将帮助人们进一步理解复制机制和相关疾病,比如癌症。
之前的高分辨率染色体构象俘获研究(Hi-C)发现,复制时间的早和晚对应着三维染色质隔间( )的开和关。而这种染色质隔间中还存在着亚结构,即拓扑相关结构域TAD。这个结构在不同细胞类型中相当保守,而且其大小与复制结构域相当。
这项研究鉴定了复制结构域的边界,明确了它们在18种人类细胞和13种小鼠细胞中的位置。总的来说,复制结构域边界与TAD边界几乎是一对一的关系。研究人员指出,TAD结构域是稳定的复制时间调控单元。
人类基因组复制的蛋白全景图
DNA的复制过程需要多种蛋白因子的协助,这些蛋白集中在复制叉附近。研究人员通过iPOND-MS技术( of on DNA with mass )分离新生DNA链上的蛋白,并对其进行综合性的蛋白质组学分析。他们解析了复制体中的蛋白组成,也鉴定了复制体附近的相关蛋白因子,找到了一些参与复制过程的新蛋白。
这是首次对复制体实现全面的蛋白组学鉴定。研究显示,这些蛋白的活性各有不同,分别负责打开DNA双螺旋、复制、修复、以及各种修饰等等。
在癌细胞中,DNA复制过程会发生异常或者变得不受控制,而这也是癌细胞的致命弱点之一。因此目前的许多化疗药物,都以DNA复制为作用目标。研究人员计划应用本研究中的新技术,进一步在DNA复制过程寻找正常细胞与癌细胞之间的差异,希望能够在此基础上开发出新的癌症治疗策略。
不同寻常的DNA复制机制
传统的DNA合成是在细胞周期的S期完成,在发现DNA结构不久后, 和 Stahl便于1958年证实了半保留DNA合成方式。他们发现两条新的DNA 双螺旋分子都分别是由一条DNA单链生成,而每个新的DNA双螺旋分子都包含一条DNA原始链和一条新链。但是随着研究的推进,越来越多不同寻常的DNA复制被发现。
一项研究表明当由于氧化、电离辐射、复制错误和某些代谢产物使得染色体经受双链断裂时,细胞会利用遗传相似的染色体通过一种涉及断裂分子两端的机制来修补这一缺口。为了修复失去一端的断裂染色体,细胞会利用DNA复制机器的一种独特构型作为一种搏命策略让细胞得以生存。
在断裂诱导复制过程中,DNA的一个断裂端会与它的伙伴染色体( )上的相同DNA序列配对。复制以一种不同寻常的气泡样模式进行,通过染色体两端的端粒由供体DNA复制出数以百万计的DNA碱基。
这种气泡样的DNA复制模式可以在不分裂细胞中运作,因此这种复制有可能是癌症形成的一条潜在途径。这一断裂诱导复制分子机制,为突变产生提供了一种新解释。
这种气泡样的DNA复制模式可以在不分裂细胞中运作,因此这种复制有可能是癌症形成的一条潜在途径。这一断裂诱导复制分子机制,为突变产生提供了一种新解释。(来源:)